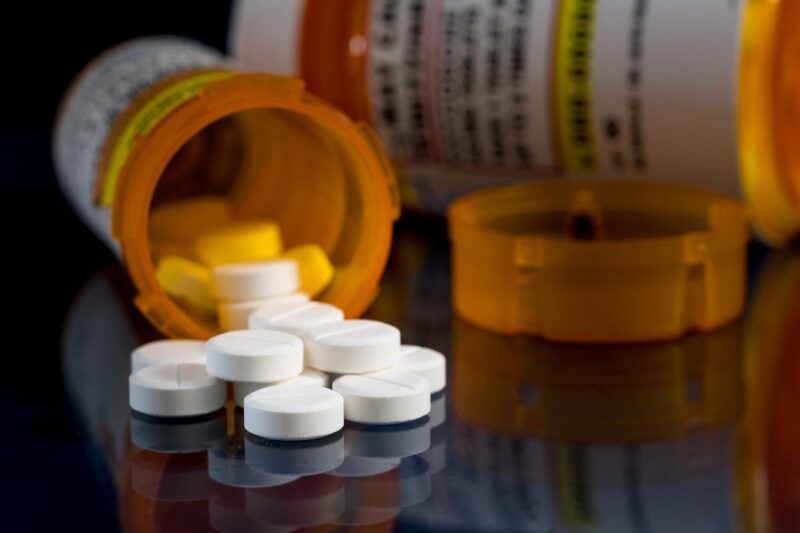
Sebuah studi baru telah mengidentifikasi senyawa baru yang dapat secara signifikan meningkatkan efektivitas nalokson, obat penyelamat nyawa yang digunakan untuk mengobati overdosis opioid. Senyawa ini membantu nalokson bekerja lebih lama dan lebih manjur, sehingga memberikan harapan dalam memerangi epidemi opioid yang sedang berkembang.
Senyawa yang baru diidentifikasi meningkatkan potensi dan durasi nalokson, menurut penelitian pada tikus.
Krisis opioid yang sedang berlangsung di AS merenggut puluhan ribu nyawa setiap tahun. Naloxone, yang dikenal dengan nama merek Narcan, telah memainkan peran penting dalam menyelamatkan banyak nyawa dengan membalikkan overdosis opioid. Namun, munculnya opioid baru yang lebih kuat telah membuat semakin sulit bagi penolong pertama untuk menyadarkan individu yang overdosis.
Kini, para peneliti telah menemukan pendekatan yang dapat memperluas kekuatan nalokson untuk menyelamatkan nyawa, bahkan dalam menghadapi opioid yang semakin berbahaya. Sebuah tim peneliti dari Fakultas Kedokteran Universitas Washington di St. Louis, Universitas Stanford, dan Universitas Florida telah mengidentifikasi obat potensial yang membuat nalokson lebih manjur dan tahan lama, membalikkan efek opioid pada tikus pada dosis rendah tanpa memperburuk gejala putus zat. Studi ini dipublikasikan pada tanggal 3 Juli di Alami.
Mekanisme dan Keterbatasan Naloxone
“Nalokson adalah penyelamat, tetapi bukan obat ajaib; obat ini punya keterbatasan,” kata penulis senior Susruta Majumdar, PhD, seorang profesor anestesiologi di University of Washington. “Banyak orang yang overdosis opioid memerlukan lebih dari satu dosis nalokson sebelum mereka terbebas dari bahaya. Studi ini merupakan bukti konsep bahwa kita dapat membuat nalokson bekerja lebih baik—bertahan lebih lama dan lebih manjur—dengan memberikannya dalam kombinasi dengan molekul yang memengaruhi respons reseptor opioid.”
Opioid seperti oksikodon dan fentanil bekerja dengan cara menyelinap ke dalam kantung reseptor opioid, yang terutama ditemukan pada neuron di otak. Keberadaan opioid mengaktifkan reseptor, memicu serangkaian peristiwa molekuler yang mengubah fungsi otak untuk sementara: mengurangi persepsi nyeri, menghasilkan perasaan euforia, dan memperlambat pernapasan. Penekanan pernapasan inilah yang membuat opioid sangat mematikan.
Senyawa molekuler yang dijelaskan dalam makalah ini adalah apa yang disebut modulator alosterik negatif (NAM) dari reseptor opioid. Modulator alosterik merupakan bidang penelitian yang sedang hangat dalam farmakologi, karena modulator ini menawarkan cara untuk memengaruhi respons tubuh terhadap suatu obat dengan menyempurnakan aktivitas reseptor obat tersebut, bukan obat itu sendiri. Rekan penulis Vipin Rangari, PhD, seorang peneliti pascadoktoral di laboratorium Majumdar, melakukan eksperimen untuk mengkarakterisasi senyawa tersebut secara kimia.
Nalokson adalah opioid, tetapi tidak seperti opioid lainnya, keberadaannya di kantong pengikat tidak mengaktifkan reseptor. Fitur unik ini memberi nalokson kekuatan untuk membalikkan overdosis dengan menggantikan opioid yang bermasalah dari kantong, sehingga menonaktifkan reseptor opioid. Masalahnya adalah nalokson hilang sebelum opioid lainnya. Misalnya, nalokson bekerja selama sekitar dua jam, sementara fentanil dapat bertahan dalam aliran darah selama delapan jam. Setelah nalokson dilepaskan dari kantong pengikat, molekul fentanil yang masih beredar dapat menempel kembali dan mengaktifkan kembali reseptor, menyebabkan gejala overdosis kembali.
Tim peneliti — yang dipimpin oleh penulis senior Majumdar; Brian K. Kobilka, PhD, seorang profesor fisiologi molekuler dan seluler di Universitas Stanford; dan Jay P. McLaughlin, PhD, seorang profesor farmakodinamik di Universitas Florida — berupaya menemukan NAM yang meningkatkan nalokson dengan membantunya bertahan di kantong pengikat lebih lama dan menekan aktivasi reseptor opioid secara lebih efektif.
Menemukan Senyawa 368
Untuk melakukannya, mereka menyaring pustaka yang berisi 4,5 miliar molekul di laboratorium untuk molekul yang akan mengikat reseptor opioid dengan nalokson yang sudah terselip di kantung reseptor. Senyawa yang mewakili beberapa keluarga molekuler berhasil melewati penyaringan awal, dengan yang paling menjanjikan dijuluki senyawa 368. Percobaan lebih lanjut dalam sel mengungkapkan bahwa, dengan adanya senyawa 368, nalokson 7,6 kali lebih efektif dalam menghambat aktivasi reseptor opioid, sebagian karena tetap berada di kantung pengikat setidaknya 10 kali lebih lama.
“Senyawa itu sendiri tidak dapat mengikat dengan baik tanpa nalokson,” kata Evan O'Brien, PhD, penulis utama penelitian dan seorang sarjana pascadoktoral di laboratorium Kobilka di Stanford. “Kami pikir nalokson harus mengikat terlebih dahulu, baru kemudian senyawa 368 dapat masuk dan menyegelnya di tempatnya.”
Yang lebih baik lagi, senyawa 368 meningkatkan kemampuan nalokson untuk membalikkan overdosis opioid pada tikus dan memungkinkan nalokson untuk membalikkan efek fentanil dan morfin pada 1/10 dosis biasa.
Namun, orang yang overdosis opioid dan sadar kembali setelah mengonsumsi nalokson dapat mengalami gejala putus zat seperti nyeri, menggigil, muntah, dan mudah tersinggung. Dalam penelitian ini, meskipun penambahan senyawa 368 meningkatkan potensi nalokson, hal itu tidak memperburuk gejala putus zat pada tikus.
“Kita masih punya jalan panjang, tetapi hasil ini menggembirakan,” kata McLaughlin. “Kemungkinan besar penghentian penggunaan opioid tidak akan membunuh Anda, tetapi efeknya sangat parah sehingga orang sering kembali menggunakan opioid dalam waktu satu atau dua hari untuk menghentikan gejalanya. Gagasan bahwa kita dapat menyelamatkan orang dari overdosis dengan penghentian penggunaan yang lebih sedikit mungkin akan membantu banyak orang.”
Senyawa 368 hanyalah salah satu dari beberapa molekul yang telah menunjukkan potensi sebagai NAM reseptor opioid. Para peneliti telah mengajukan paten pada NAM, dan berupaya untuk mempersempit dan mengkarakterisasi kandidat yang paling menjanjikan. Majumdar memperkirakan bahwa akan butuh 10 hingga 15 tahun sebelum NAM peningkat nalokson dipasarkan.
“Mengembangkan obat baru adalah proses yang sangat panjang, dan sementara itu, opioid sintetis baru bermunculan yang semakin kuat, yang berarti semakin mematikan,” kata Majumdar. “Harapan kami adalah dengan mengembangkan NAM, kami dapat mempertahankan kekuatan nalokson untuk bertindak sebagai penawar racun, apa pun opioid yang muncul di masa mendatang.”
Referensi: “Modulator reseptor µ-opioid yang bekerja sama dengan nalokson” oleh Evan S. O'Brien, Vipin Ashok Rangari, Amal El Daibani, Shainnel O. Eans, Haylee R. Hammond, Elizabeth White, Haoqing Wang, Yuki Shiimura, Kaavya Krishna Kumar, Qianru Jiang, Kevin Appourchaux, Weijiao Huang, Chensong Zhang, Brandon J. Kennedy, Jesper M. Mathiesen, Tao Che, Jay P. McLaughlin, Susruta Majumdar dan Brian K. Kobilka, 3 Juli 2024, Alami.
DOI: 10.1038/s41586-024-07587-7
Penelitian ini didanai oleh American Diabetes Association, American Heart Association, Institut Kesehatan Nasionaldan Inisiatif Chan Zuckerberg.
NewsRoom.id